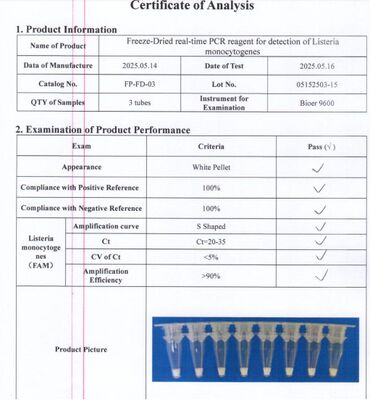
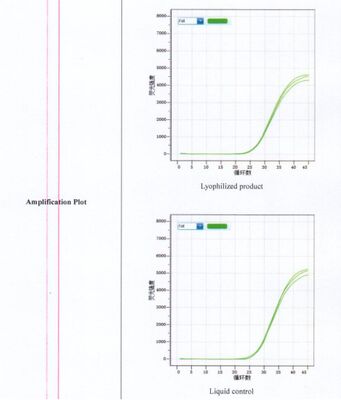
LyoDt® Reagente per la rilevazione PCR in tempo reale liofilizzato per Listeria monocytogenes
Uso’Manuale
1. DESCRIZIONE
Listeria monocytogenes, un piccolo bacillo Gram-positivo, è un patogeno zoonotico trasmesso principalmente per via oro-fecale. Inoltre, può entrare nel corpo attraverso il contatto oculare o la pelle/membrane mucose lesionate. L'infezione si manifesta tipicamente come setticemia, meningite e monocitosi.
Questo prodotto è un reagente PCR in tempo reale liofilizzato per la rilevazione di Listeria monocytogenes< Utilizza il gene altamente conservato hlyA di Listeria monocytogenes come bersaglio di rilevazione. È un mastermix contenente tutti gli ingredienti necessari, ad eccezione del DNA modello, ed è pre-dosato come singolo test in provette PCR per un facile utilizzo. Questo prodotto non richiede la catena del freddo per il trasporto e lo stoccaggio, il che riduce significativamente i costi di spedizione ed elimina possibili perdite dovute allo spreco di reagenti e alla contaminazione da aerosol.
2. SPECIFICHE E COMPOSIZIONE
|
Cat. No.
|
Descrizione
|
QTÀ
|
|
FP-FD-03
|
LyoDt® Reagente per la rilevazione PCR in tempo reale liofilizzato per Listeria monocytogenes
|
48 Test
|
|
FP-FD-03PC
|
Controllo positivo
|
9 Provette
|
|
EP-CM-10
|
Sacchetto di plastica richiudibile
|
1 sacchetto
|
3. CONSERVAZIONE E DURATA
Conservare a temperatura ambiente (5-3045. Se le provette fornite non sono compatibili con lo strumento, trasferire il pellet di reagente in una provetta ottica compatibile con lo strumento.< È stabile fino a 12 mesi< Una volta aperto l'imballaggio sottovuoto, conservare i prodotti inutilizzati nel sacchetto di plastica richiudibile fornito con i disidratanti, e nel sacchetto di alluminio.
ATTENZIONE:
La riduzione del pellet di reagente è un'indicazione dell'infiltrazione di umidità nella provetta e il reagente è inumidito. Eventuali reagenti con dimensioni del pellet significativamente inferiori al solito devono essere scartati o testati con il controllo positivo prima dell'uso per il test del campione.
4. ATTREZZATURE E REAGENTI AGGIUNTIVI NECESSARI
1) Strumento PCR in tempo reale
2) Pipette e puntali
PCR in tempo reale Acqua priva di-nucleasi
Impostazione RT-PCRKit di estrazione degli acidi nucleici
5. SISTEMI PCR IN TEMPO REALE COMPATIBILI
ABI 7500/Fast, Roche LightCycler 480II, BioRad CFX96, Bioer LineGene 9600<
6. CAMPIONI ACCETTABILI
Brodo di arricchimento alimentare, vomito, campioni di diarrea, ecc.
7. PROCEDURA OPERATIVA
1) Nucleico e cido Estrazione
Estrarre DNA dai campioni utilizzando un kit di estrazione appropriato. Si raccomanda che il DNA venga eluito con circa 100μl di tampone di eluizione Tagliare il numero di provette necessarieTE o H priva di nucleasiO, O. Se le provette fornite non sono compatibili con lo strumento, trasferire il pellet di reagente in una provetta ottica compatibile con lo strumento. nella fase finale di estrazione. L'acido nucleico purificato deve essere utilizzato immediatamente o conservato a -20°C.
2) Preparazione del controllo positivo
Il controllo positivo può essere conservato a temperatura ambiente prima della reidratazione fino a 12 mesi. Deve essere reidratato prima dell'uso aggiungendo 250 μl di tampone TE o H priva di nucleasi2O, vortexato a bassa velocità per 15-20 secondi e centrifugato a bassa velocità per 15-20 secondi. Utilizzare immediatamente o conservare a -20°C45<
PCR in tempo reale Mix PreparazioneA) Aprire l'imballaggio sottovuoto ed estrarre la striscia a 8 provette
s contenente il reagente. Verificare che il pellet sia sul fondo della provetta( Tagliare il numero di provette necessariese necessario). Se le provette fornite non sono compatibili con lo strumento, trasferire il pellet di reagente in una provetta ottica compatibile con lo strumento.B) Aprire le provette e scartare il/i tappo/i (non adatto/i per le macchine PCR in tempo reale) e preparare il mix di reazione su ghiaccio come di seguito.
Componente
|
Vol. /test
|
Reagente liofilizzato
|
|
1
|
provette (2μl)Modello
|
|
DNA/Controllo positivo/Controllo negativo*23μl
|
Totale
|
|
25μl
|
* L'acqua priva di nucleasi può essere utilizzata come controllo negativo.
|
C)
Tappare la PCR utilizzando tappi (strisce) adatti per PCR in tempo reale(non forniti).D) Vortexare le provette a bassa velocità per 10~15 secondi e centrifugare a 3000 giri/min per 20 secondi e posizionarle in uno strumento PCR in tempo reale.
4)
Impostazione RT-PCRImpostare il volume di reazione a 25μl e la procedura di amplificazione PCR come di seguito. Raccogliere la fluorescenza FAM a 60°C e selezionare NESSUNO come riferimento passivo.
Passaggio Temp.
|
Tempo
|
Cicli
|
Pre-denaturazione
|
9
|
|
4
|
°C5) 45
|
1Amplificazione
|
9
|
|
4
|
°C5) 45
|
60°C
|
4
|
|
0sec
|
5) Risultato
|
Analisi e Interpretazione Modello
|
CTInterpretazione
|
Contaminazione incrociata, esperimento non valido.
|
CT≤35
|
|
Reagente buono.
|
positivo
|
CT>40 o nessun CT
|
|
Nessuna contaminazione, esperimento valido.
|
negativo.
|
<35
|
|
Contaminazione incrociata, esperimento non valido.35
|
|
|
CCampione
|
CT≤35
|
|
Listeria
|
positivo
|
35<
|
|
CT≤40Listeriasospetto, confermare ritestando.
|
Listeria
|
|
negativo.
|
|

 Il tuo messaggio deve contenere da 20 a 3000 caratteri!
Il tuo messaggio deve contenere da 20 a 3000 caratteri! Si prega di controllare la tua email!
Si prega di controllare la tua email!  Il tuo messaggio deve contenere da 20 a 3000 caratteri!
Il tuo messaggio deve contenere da 20 a 3000 caratteri! Si prega di controllare la tua email!
Si prega di controllare la tua email!